- Оксид бора
-
Оксид бора 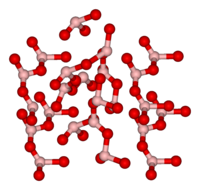
Общие Систематическое наименование оксид бора Химическая формула B2O3 Физические свойства Состояние (ст. усл.) бесцв. стеловидная масса Отн. молек. масса 69.6182 а. е. м. Молярная масса 69.6182 г/моль Плотность 1.85 (стекл.);
2.460 г/мл3 (жид.) г/см³
Термические свойства Температура плавления 480 °C °C Температура кипения 1680 °C °C Химические свойства Растворимость в воде 2.2 г/100 мл Классификация Рег. номер CAS [1303-86-2] Безопасность Токсичность
Окси́д бо́ра B2O3 — ангидрид борной кислоты, бесцветное, довольно тугоплавкое стекловидное или кристаллическое вещество горьковатого вкуса, диэлектрик.Стеклообразный оксид бора имеет слоистую структуру (расстояние между слоями 0.185 нм), в слоях атомы бора расположены внутри равносторонних треугольников ВО3 (d В—О=0.145 нм). Эта модификация плавится в интервале температур 325—450 °C и обладает высокой твёрдостью. Она получается при нагревании бора на воздухе 700 °C или обезвоживанием ортоборной кислоты. Кристаллический В2О3, который получают осторожным отщеплением воды от метаборной кислоты НВО2, существует в двух модификациях — с гексагональной кристаллической решёткой, при 400 °C и 2200 МПа переходящей в моноклинную.
Содержание
Свойства
- Борный ангидрид гигроскопичен, он бурно растворяется в воде, образуя вначале различные метаборные кислоты общей формулы (НВO2)n. Дальнейшее оводнение приводит к образованию ортоборной кислоты H3BO3.
- Расплавленный B2O3 хорошо растворяет оксиды многих элементов. С оксидами металлов образует соли бораты.
- B2O3 является кислотным ангидридом, проявляя также очень слабые признаки амфотерности:
- Сам оксид бора не восстанавливается углеродом даже при температуре белого каления, однако разлагается, если одновременно ввести в реакцию вещества, способные заместить кислород (хлор или азот):
- При нагревании оксида бора с элементарным бором выше 1000о в парах существуют термически устойчивые линейные молекулы O=B—B=O. При быстром охлаждении паров ниже 300о может быть получен белый твёрдый полимер состава (B2O2)n, не имеющий определённой точки плавления и сильно реакционноспособный. Под давлением в 60 тыс. ат. и температуре 1500о оксид бора взаимодействует с элементарным бором по реакции:
-
- Этот низший оксид бора имеет графитоподобную слоистую структуру.
Получение
Образуется при нагревании бора в атмосфере кислорода или на воздухе
А также при обезвоживании борной кислоты:
Применение
Эфиры борной кислоты. Используется в качестве флюса.
Литература
- Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия. М.: Химия 1994
- Реми Г. «Курс неорганической химии» М.: Иностранная литература, 1963
 Соединения бора
Соединения бораАрсенид бора (BAs) • Боразол (B3N3H6) • Борная кислота (H3BO3) • Борогидрид натрия (NaBH4) • Диборан (B2H6) • Карбид бора (B4C) • Метаборат натрия (NaBO2) • Нитрид бора (BN) • Оксид бора (B2O3) • Пентаборат натрия (NaB5O8) • Субоксид бора (B6O) • Сульфид бора (B2S3) • Тетраборан (B4H10) • Тетраборат натрия (Na2B4O7) • Тетрагидридоборат лития (Li[BH4]) • Тетрафторид бора (B2F4) • Тетрафтороборат водорода (H[BF4]) • Тетрафтороборат натрия (Na[BF4]) • Трибромид бора (BBr3) • Трииодид бора (BI3) • Трифторид бора (BF3) • Трихлорид бора (BCl3) • Фосфид бора (BP)
Категории:- Соединения бора
- Солеобразующие оксиды
- Диэлектрики
- Твёрдое тело
Wikimedia Foundation. 2010.







